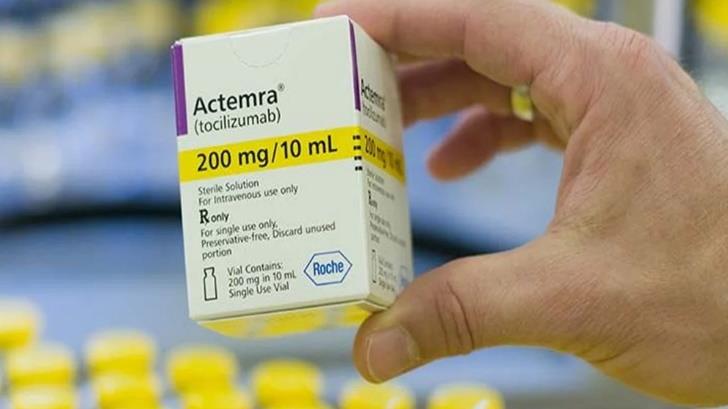
Alertan sobre falsificación de medicamentos contra artritis
La Comisión Estatal contra Riesgos Sanitarios alertó a la población sobre la falsificación de medicamentos indicados para el tratamiento de la artritis reumatoide (AR) activa.
CULIACÁN, SIN.- La Comisión Estatal contra Riesgos Sanitarios alertó a la población sobre la falsificación de medicamentos indicados para el tratamiento de la artritis reumatoide (AR) activa, de intensiva moderada a grave, en pacientes adultos, así como en el tratamiento de la artritis idiopática juvenil y sistémica en niños a partir de los dos años.
Jorge Alan Urbina Vidales, titular de la dependencia, replicó en el estado la información divulgada a nivel nacional sobre la falsificación del Roactemna (tocilizumab) en solución.
A través de una denuncia interpuesta por la empresa Productos Roche, S.A. de C.V para el producto RoActemra, solución 80mg/4mL inyectable M:B, caja con un frasco ámpula de 4mL, y Roactemra solución 200mg/0mL, caja con un frasco ámpula de 10mL.
El funcionario estatal recomendó a la población que antes de adquirir estos medicamentos inspeccione el etiquetado del mismo, su contenido y, en caso de identificar uno de los lotes reportados, no adquirirlos.
Alan Urbina comentó que la empresa realizó análisis comparativos de estos productos concluyendo que los recuperados son falsos por lo que presentó la denuncia respectiva.
La Comisión Estatal de Protección contra Riegos Sanitarios orientó a la población que requiere de estos tratamientos revisar que estos no correspondan a los lotes B2080804 y 82096B03, con fecha de caducidad el 17 de abril del 2021, en la presentación de solución 80mg/4mL inyectable MB, caja con un frasco ámpula de 4mL.
Así como del lote B2078801, con fecha de caducidad el 24 de Octubre del 2020, de la presentación solución 200mg/10mL, caja con un frasco ámpula de 10mL.
Los análisis practicados por la empresa Roche a los productos, que llevan etiquetados dicha guías de lotes en los empaques de las cajas de cartón, carecen de dos leyendas impresas, los pegamentos adicionales en la solapa interior secundario no presentan los insertos correspondientes a los instructivos para el usuario y para el profesional de salud.
En el empaque primario (vial), el tamaño del tapón de plástico del vial es mayor con respecto al original, se observó daños en el casquillo de la tapa a nivel del sujetador, las piezas recuperadas no cuentan con etiqueta de identificación.
Los contenidos líquidos en el vial son menores o mayores a los originales y se trata de una sustancia incolora con presencia de sólidos con apariencia de crecimiento de microbiano o liquido colorido.
Finalmente, el funcionario estatal externó que las farmacias y puntos de venta de medicamentos deben adquirirlos a través de distribuidores autorizados y en este caso, se les solicitó que verifiquen sus existencias y cotejen la información dada a conocer.